Ankylbenzen là gì? Cấu tạo và ứng dụng của Benzen như thế nào? Đây là khái niệm các bạn đã được học ở môn Hóa lớp 11. Trong bài viết này Mindovermetal sẽ ôn tập lại các kiến thức liên quan đến Ankylbenzen và Benzen.
Mục lục nội dung
Ankylbenzen là gì?
Ankylbenzen thực chất là đồng đẳng của benzen, bao gồm các hiđrocacbon có chứa gốc ankyl và 1 vòng benzen. Có công thức chung là CnH2n – 6 (n ⩾ 6).
Từ C8H10 trở lên (n > 8), Ankylbenzen xuất hiện đồng phân mạch cacbon. Trong đó, các gốc hidrocacbon sẽ biến đổi xung quanh vòng benzen.
Danh pháp
- Dạng 1 nhánh: gốc ankyl + benzen
- Dạng 2 hay nhiều nhánh: Tên vị trí – tên nhánh + benzen

Cấu tạo của Benzen
Công thức hóa học: C6H6
Phân tử benzen bao gồm 6 nguyên tử C tạo thành hình lục giác đều. Trong đó, mỗi nguyên tử C được liên kết với một nguyên tử H, và độ dài của các liên kết sẽ bằng nhau. Tất cả các nguyên tử đều nằm trên một mặt phẳng.
Tính chất của Benzen
Tính chất vật lý
- Hiđrocacbon thơm là chất lỏng hoặc rắn ở điều kiện thường, chúng có nhiệt độ sôi tăng theo chiều tăng của phân tử khối
- Benzen và ankylbenzen là những chất không màu, có mùi đặc trưng, và hầu như không tan được trong nước nhưng tan nhiều trong dung môi hữu cơ. Ví dụ: benzen hòa tan iot, lưu huỳnh, brom, cao su, chất béo,…
- Benzen dễ cháy ở nhiệt độ thường. Khi benzen cháy sẽ tạo ra khí CO2 và nước, đặc biệt có sinh ra muội than
Tính chất hóa học
Phản ứng thế
1. Phản ứng với halogen
Cho benzen và brom vào ống nghiệm khô rồi lắc nhẹ hỗn hợp và để yên. Vì benzen không tác dụng với nước brom, nên chất lỏng trong ống nghiệm sẽ tách thành 2 lớp: lớp chất lỏng trên là dung dịch brom trong benzen có màu vàng, và lớp dưới là nước trong suốt.
Tiếp theo, cho một ít bột sắt vào ống nghiệm chứa hỗn hợp benzen và brom, lắc nhẹ rồi để yên. Lúc này, màu của brom sẽ nhạt dần và tạo thành khí Hidro bromua và brombenzen. Do đó xảy ra phản ứng thế:
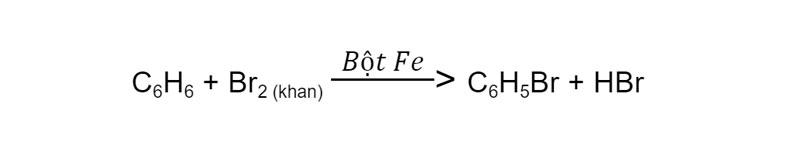
Nếu cho các ankylbenzen phản ứng với brom trong điều kiện có bột sắt. Lúc này sẽ thu được hai hỗn hợp đồng phân ortho và para.
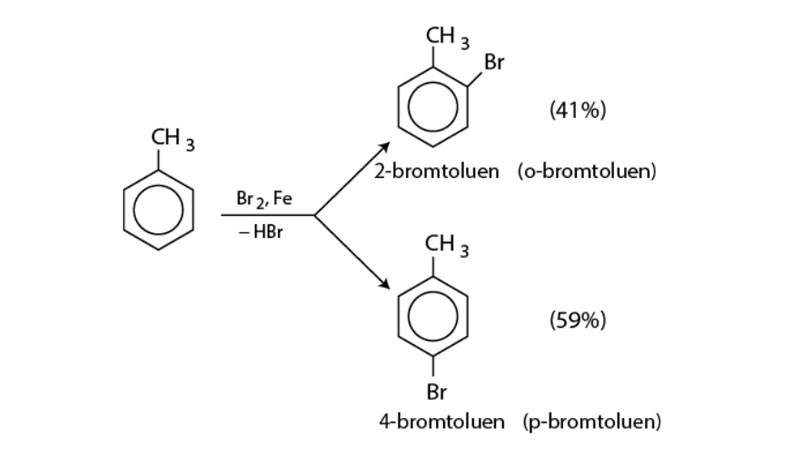
Nếu không dùng sắt mà thay vào đó là điều kiện ánh sáng. Trong trường hợp này, brom sẽ thay thế cho H ở nhánh. Có cấu trúc như sau:
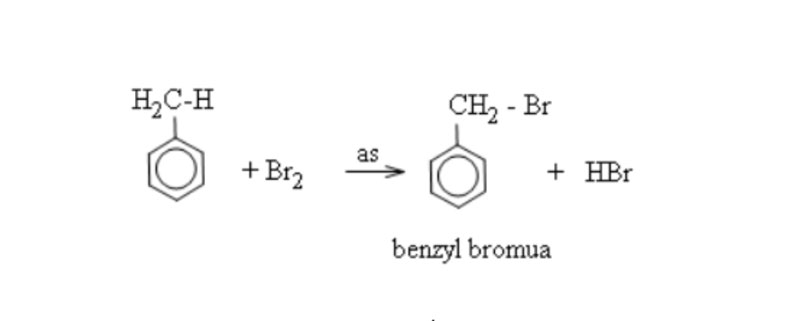
2. Phản ứng với Axit Nitric
Benzen phản ứng với hỗn hợp HNO3 đặc và H2SO4 đặc tạo thành Nitrobenzen.
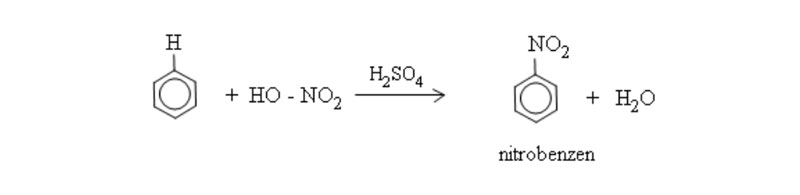
Nitrobenzen tác dụng với hỗn hợp HNO3 bốc khói và H2SO4 đậm đặc. Sau đó đun nóng sẽ tạo thành m-đinitrobenzen.
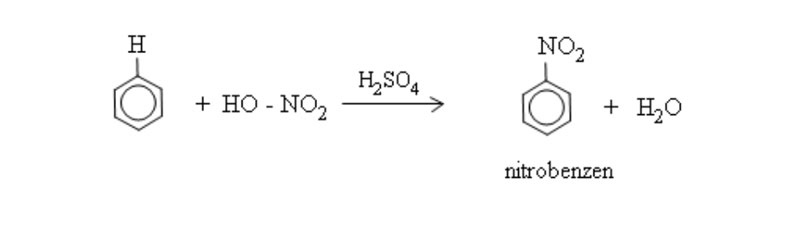
Toluen tham gia phản ứng dễ dàng hơn (chỉ cần HNO3 đặc không cần bốc khói) tạo hỗn hợp sản phẩm ortho và para.
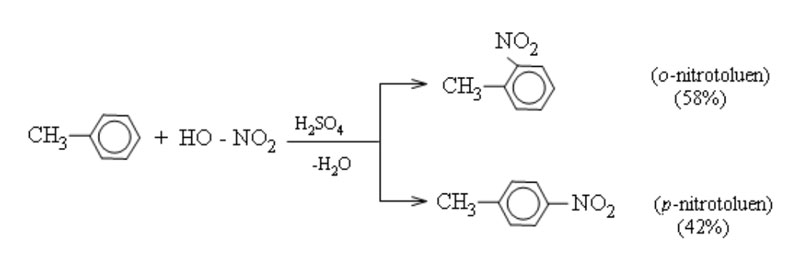
3. Quy tắc thế ở vòng Benzen
Nếu ở vòng benzen có sẵn nhóm ankyl (hay các nhóm -OH, -NH2, -OCH3, -NR,…), phản ứng thế vào vòng sẽ dễ dàng hơn và ưu tiên ở vị trí ortho và para.
Ngược lại, nếu vòng benzen đã có sẵn nhóm -NO2 (hoặc các nhóm –COOH, -SO3H, -CHO…) phản ứng thế vào vòng sẽ khó hơn và ưu tiên xảy ra ở vị trí meta.
Phản ứng cộng
1. Cộng hiđro
Trong khi đun nóng mà có chất xúc tác Ni hay Pt, benzen và ankylbenzen cộng với hiđro tạo thành xicloankan.
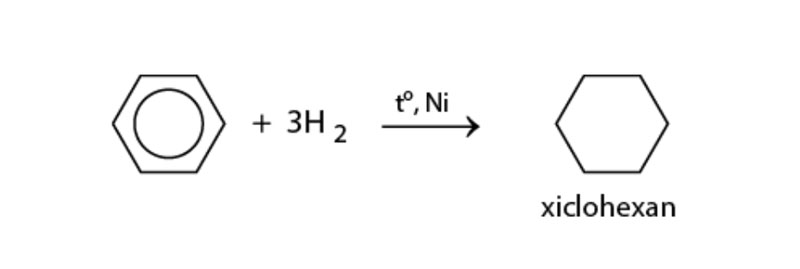
2. Cộng halogen
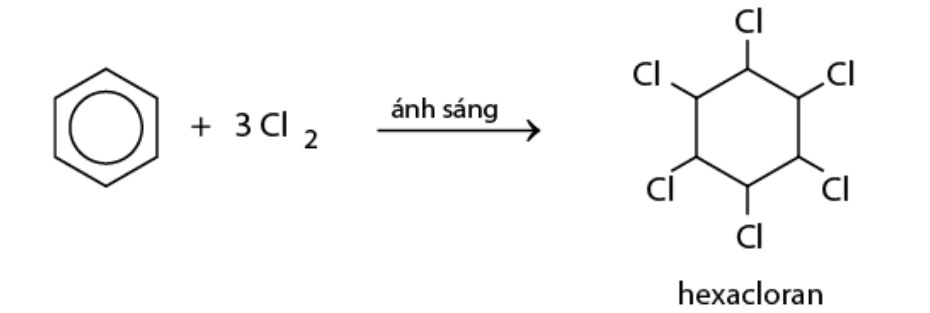
Dẫn lượng nhỏ khí Cl2 vào bình chứa một ít benzen, đậy kín lại rồi đưa bình ra ngoài ánh nắng. Lúc này, trong bình sẽ xuất hiện khói trắng và thành bình có một lớp bột màu trắng. Đó chính là hexacloran (hay còn gọi là thuốc trừ sâu 666).
Phản ứng Oxi hóa
1. Phản ứng Oxy hóa hoàn toàn
Các hiđrocacbon thơm khi cháy sẽ toả nhiều nhiệt.
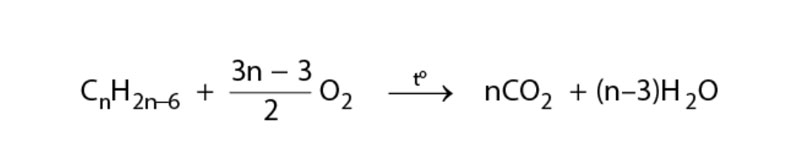
2. Phản ứng Oxy hóa không hoàn toàn
Benzen không tác dụng được với KMnO4 chính vì vậy mà chúng sẽ không làm mất màu dung dịch KMnO4.
Benzen cũng rất dễ cháy và tạo ra khí cacbon đioxit và hơi nước. Hơn nữa, Benzen khi cháy trong không khí thì chúng còn tạo ra muội than.
Các ankylbenzen khi đun nóng với dung dịch KMnO4 thì chỉ có nhóm ankyl bị oxi hóa.
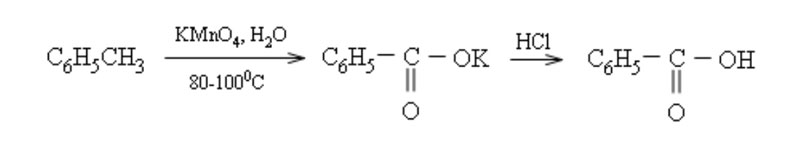
Ứng dụng Benzen trong đời sống
- Benzen được sử dụng rất phổ biến trong đời sống, đặc biệt là ngành công nghiệp hóa hữu cơ. Chúng được dùng trong sản xuất polyme làm chất dẻo, tơ sợi, cao su.
- Các nhà thí nghiệm dùng benzen để điều chế ra các chất khác. Ví dụ như: axeton, anilin, phenol, nitrobenzen, dược phẩm, tổng hợp phẩm nhuộm, thuốc trừ dịch hại,…
- Benzen cũng được dùng để tẩy mỡ ở xương, da sợi, vải, len, dạ, các tấm kim loại, và các dụng cụ có bám chất mỡ.
Như vậy, chúng tôi đã tổng hợp tất tần tật về Ankylbenzen là gì? Hy vọng các bạn sẽ áp dụng những kiến thức trên thật tốt trong các chương trình học. Hãy theo dõi Mindovermetal để cập nhập thêm nhiều thông tin bổ ích nhé! Chúc các bạn thành công.